أمراض وراثية
تعريف
المرض الوراثي أو المرض الوراثي هو مرض يسببه جين واحد أو أكثر للشخص المعني. يعمل الحمض النووي هنا كمحفز مباشر للمرض. بالنسبة لمعظم الأمراض الوراثية ، فإن مواقع الجينات المسببة معروفة. في حالة الاشتباه في وجود مرض وراثي ، يمكن إجراء التشخيص المناسب من خلال الفحص الجيني.
من ناحية أخرى ، هناك أيضًا عدد من الأمراض التي يكون لحدوثها تأثير وراثي أو تتم مناقشته ، مثل داء السكري ("السكري") أو هشاشة العظام أو الاكتئاب. هذه هي ما يسمى التصرفات ، أي زيادة احتمال الإصابة بأمراض معينة. يجب تمييز التصرفات عن الأمراض الوراثية.

هذه أمراض وراثية شائعة
من حيث القيمة المطلقة ، فإن الأمراض الوراثية ليست شائعة ، ولكن الأمراض الوراثية المذكورة هنا تحدث كثيرًا مقارنة بالأمراض الأخرى ذات الأسباب الوراثية.
-
متلازمة مارفان
-
فقر الدم المنجلي
-
الهيموفيليا (الهيموفيليا A أو B)
-
طفرة العامل الخامس ليدن ومقاومة APC الناتجة
-
ضعف الأحمر والأخضر
-
نقص نازعة الجلوكوز 6 فوسفات (نقص G6PD)
-
كثرة الأصابع ("تعدد الأصابع" ، يمكن أيضًا أن تكون أحد أعراض الأمراض الأخرى)
-
تثلث الصبغي 21 (متلازمة داون)
-
رقص هنتنغتون
الأسباب
الأمراض الوراثية متنوعة للغاية في مظهرها. لديهم في الأساس شيء واحد مشترك: السبب وراء كل منهم يكمن في الحمض النووي ، أي في المادة الجينية للشخص المعني. يمكن أن تحدث تغييرات مختلفة هنا ، مثل الطفرات (تبادل معلومات الحمض النووي) أو الحذف (نقص مادة وراثية معينة).
يتم ترميز كمية كبيرة من المعلومات في المادة الجينية ، مثل "المخططات" لمكونات مختلفة مهمة لعمل خلية الجسم. يمكن أن تكون هذه إنزيمات أو قنوات إلكتروليت أو مواد مرسال ، على سبيل المثال. ثم تُقرأ هذه العناصر الأصغر بشكل غير صحيح أو لا تقرأ على الإطلاق من الحمض النووي ، والذي يكون مفقودًا بعد ذلك في النظام المعقد للجسم. وبالتالي فإن المعلومات الجينية الخاطئة أو المفقودة تسبب بعض الأعطال في الجسم. ثم تسبب هذه الأعراض وفقًا للنظام الوظيفي الذي يفتقد فيه عنصر واحد الآن.
اكتشف كل شيء عن الموضوع هنا: الاختبار الجيني.
هذه هي الطريقة التي يتم بها توريث الأمراض الوراثية
يتم توريث كل مرض وراثي إما بشكل أحادي أو متعدد الجينات: وهذا يعني أن هناك موقعًا جينيًا واحدًا أو أكثر يجب تغييره ليؤدي إلى الإصابة بمرض.
علاوة على ذلك ، يمكن دائمًا توريث السمات الوراثية بطريقة سائدة أو متنحية: المتنحية تعني أنه يجب أن يكون هناك استعداد لهذا المرض الوراثي المعين في كل من جينات الأب والأم. في حالة الوراثة السائدة ، يكفي تغيير واحد (أي أحد الوالدين) لإحداث المرض. ويترتب على ذلك أنه مع الأمراض الوراثية السائدة ، فإن الأشخاص الذين يحملون المرض سيصابون أيضًا بالمرض - بينما مع الوراثة المتنحية ، لا يُعرف عادةً وجود استعداد وراثي مماثل.
هناك أيضًا أمراض موروثة من الكروموسومات الجنسية ، مثل الهيموفيليا أو العمى الأحمر والأخضر. عادةً ما تكون التسهيلات الخاصة بذلك على الكروموسوم X ، نظرًا لأن الكروموسوم Y صغير جدًا بشكل عام ويمكنه عمومًا تخزين القليل من المعلومات الجينية. لذلك يتحدث المرء عن الأمراض الوراثية المرتبطة بالكروموسوم X. عادة ما تؤثر هذه على الرجال أكثر بكثير من النساء ، حيث يمكن للمرأة تعويض أي معلومات غير صحيحة عن الكروموسوم X بالثاني.
عادة ما يكون من السهل البحث عن كيفية وراثة مرض وراثي بالضبط إذا كنت مهتمًا.
اختبارات قبل الولادة
من حيث المبدأ ، يمكن بالفعل فحص المادة الوراثية للطفل في الرحم بحثًا عن جميع الأمراض الوراثية المعروفة مواقعها الجينية المسببة. ومع ذلك ، فإن التحليلات الجينية تستغرق وقتًا طويلاً ، لذلك عادةً ما يتم تحليل موقع الجين المشتبه فيه فقط - ولهذا ، بدوره ، يجب أن يكون هناك شك مبرر في وجود مرض وراثي.
لإجراء مثل هذا الفحص ، يمكن بعد ذلك أخذ المادة الوراثية من السائل الأمنيوسي أو المشيمة واستخدامها في التحليل.
ومع ذلك ، يجب دائمًا ألا يغيب عن البال أن أي تشخيص باضع ينطوي أيضًا على خطر على حياة الطفل الذي لم يولد بعد. لذلك يجب وزن هذه الثقوب على حدة في كل حالة.
هناك أيضًا قياسات يمكن أن تشير إلى مرض وراثي ، مثل قياس شفافية مؤخرة العنق كعلامة على التثلث الصبغي 21. هذه الطرق ليست خطيرة على الجنين ، ولكنها لا تقدم اليقين المطلق بوجود مرض وراثي. لذلك هنا أيضًا ، يجب النظر بعناية في العملية.
التثلث الصبغي 21
سبب التثلث الصبغي 21 هو الكروموسوم 21 ، والذي لا يوجد مرتين ولكن ثلاث مرات في الأشخاص المصابين. يتم إنشاء هذا البديل من الحمض النووي عندما يتم توزيع الكروموسومات في الخلايا الجرثومية الأبوية ، أي الحيوانات المنوية أو خلايا البويضة. لذلك فهو "خطأ توزيع" وليس تغيير في المادة الجينية الفعلية. وهذا يفسر سبب حدوث التثلث الصبغي 21 تلقائيًا في كل عائلة ولماذا يكون احتمال إنجاب طفل مصاب بمتلازمة داون هو نفسه في جميع العائلات. بالمعنى الدقيق للكلمة ، لا ينبغي اعتبار التثلث الصبغي 21 - مثل التثلث الصبغي الآخر - مرضًا وراثيًا بالمعنى الحقيقي. ومع ذلك ، فإن التثلث الصبغي 21 هو أكثر الأمراض المرتبطة بالحمض النووي شيوعًا عند الأطفال حديثي الولادة.
يمكن بالفعل رؤية سمات المجموعة المتغيرة من الكروموسومات في متلازمة داون لدى الجنين في الرحم: يمكن أن يؤدي تأخر النمو والعيوب إلى جمجمة صغيرة جدًا وقصر عظام الفخذ والذراع العلوي وعيوب في القلب. يمكن أيضًا أن تكون كمية كبيرة من السائل الأمنيوسي مؤشرًا على التثلث الصبغي 21 ، حيث يشرب الأطفال الذين لم يولدوا بعد أو يبتلعوا القليل نسبيًا من السائل الأمنيوسي. ومع ذلك ، لا تعتبر أي من هذه السمات علامات نهائية لمتلازمة داون!
بالإضافة إلى علامات تأخر النمو المذكورة ، غالبًا ما يظهر الأطفال المصابون بمتلازمة داون تأخرًا في النمو ، على سبيل المثال في مجالات اللغة والمهارات الحركية. غالبًا ما يظهر الأشخاص المصابون بمتلازمة داون مهارات اجتماعية ملحوظة ، بينما يظل الذكاء غالبًا أقل من المتوسط. ومع ذلك ، يختلف الأشخاص المصابون اختلافًا كبيرًا في هذه الخصائص ، وليس من غير المألوف أن يتخرجوا من المدرسة بعد تلقي دعم جيد.
في وقت لاحق من الحياة ، يكون الأشخاص المصابون بالتثلث الصبغي 21 أكثر عرضة للإصابة بأمراض معينة. وتشمل مرض الزهايمر والصرع والسرطان ، وخاصة اللوكيميا. ومع ذلك ، يستمر متوسط العمر المتوقع للأشخاص ذوي متلازمة داون في الارتفاع: في هذه الأثناء ، غالبًا ما يصل الأشخاص المصابون إلى سن 60 أو 70.
يمكنك العثور على مزيد من المعلومات على موقعنا متلازمة داون
نقص ألفا 1 أنتيتريبسين
يمكن أن يتخذ نقص ألفا -1 أنتي تريبسين أشكالًا وأشكالًا مختلفة ، اعتمادًا على الخصائص الجينية الدقيقة للشخص المصاب. هذا يعني أنه ليس كل نقص في ألفا -1 أنتيتريبسين يؤدي إلى أعراض. في ما يلي ، سيتم فقط مناقشة النوع الواضح سريريًا (PiZZ) لهذا المرض المحدد وراثيًا.
يتسبب عيب الإنزيم الموجود في هذا المرض في انهيار وإعادة تشكيل اللبنات الأساسية في أنسجة العضو لدى الأشخاص المصابين. بالإضافة إلى ذلك ، يتم تصفية البروتينات المعيبة من الدم عن طريق الكبد وتتراكم هناك. يمكن أن يؤدي ذلك إلى التهاب الكبد (التهاب الكبد) أو تليف الكبد أو سرطان الكبد. تصبح الممرات الهوائية في الرئتين غير مستقرة بسبب نقص الأنسجة المستقرة وتنهار بسرعة أكبر: تتطور الصورة السريرية لمرض الانسداد الرئوي المزمن (مرض الانسداد الرئوي المزمن). غالبًا ما تكون هذه الصورة السريرية هي أول أعراض نقص مضاد التريبسين alpha-1 ، لذلك يجب فحص أي شخص مصاب بمرض الانسداد الرئوي المزمن في سن أصغر بحثًا عن نقص alpha-1 antitrypsin.
إذا استمر المرض لفترة طويلة ، فقد تنتفخ الرئتان بشكل مفرط ، لأن الهواء الذي تتنفسه لا يمكن زفيره بشكل صحيح عبر الممرات الهوائية غير المستقرة ويتراكم في الرئتين. كعلاج ، بالإضافة إلى تجنب تدخين السجائر باستمرار والتطعيمات المنتظمة للوقاية من أمراض الجهاز التنفسي ، يجب أيضًا اتخاذ تدابير طبية: يمكن إعطاء alpha-1-antitrypsin المفقود عن طريق الوريد لتخفيف الأعراض قدر الإمكان ووقف مسار المرض.
يمكنك العثور على مزيد من المعلومات على موقعنا نقص ألفا 1 أنتيتريبسين
الهيموفيليا
تُعرف مجموعة الهيموفيليا أيضًا بالعامية باسم "الهيموفيليا" ، حيث يصف هذا المصطلح الأعراض الرئيسية لهذا المرض الوراثي بدقة شديدة: ينزف المصابون لفترة أطول ، اعتمادًا على شدة المرض ، في كثير من الأحيان أكثر من غير مصابين.
يتم إيقاف النزيف عادةً من خلال ما يُعرف باسم شلال التخثر ، وهو مسار إشارات داخلي يمنع فقدان الدم المفرط. في نظام التخثر هذا ، هناك 13 عاملاً يلعب دورًا ، والتي تنشط بعضها البعض الواحد تلو الآخر. يمكن تخيل هذا كسلسلة من قطع الدومينو: إذا اصطدمت بحجر واحد (عامل التخثر) ، فإنه ينشط الحجر التالي ، وهكذا. في نهاية مسار الإشارة هذا أو الدومينو يوجد تخثر للدم. مع الهيموفيليا ، هناك عامل مفقود - اعتمادًا على النوع الفرعي المحدد للمرض: ينقطع التفاعل التسلسلي هنا.
يمكن إجراء علاج المرض عن طريق تحديد العامل المفقود وإضافته من الخارج. لذلك يجب على الأشخاص المتأثرين حقن أنفسهم بانتظام بمستحضر باستخدام عامل التخثر هذا حتى يمكن حدوث بقية التفاعل التسلسلي.
يمكنك العثور على مزيد من المعلومات على موقعنا أمراض الدم
تليف كيسي
في مرض التليف الكيسي الوراثي - المعروف أيضًا باسم التليف الكيسي - هناك خلل في إنتاج القنوات الأيونية ، وبشكل أكثر دقة لقنوات الكلوريد. ونتيجة لذلك ، يتغير تكوين إفرازات الجسم (مثل العرق والإفرازات من الجهاز التنفسي والبنكرياس) للشخص المصاب: نظرًا لأن نقص الكلوريد يعني سحب كمية أقل من الماء إلى قناة الغدة المعنية ، يكون الإفراز سميكًا نسبيًا.
نتيجة لذلك ، تظهر الأعراض عادة في الجهاز الهضمي ، حيث لا يمكن أن يتدفق إفراز الإنزيمات الهضمية بشكل جيد من البنكرياس إلى الأمعاء وبالتالي يتلف البنكرياس نفسه. بالإضافة إلى ذلك ، فإن اضطرابات الجهاز الهضمي مثل البراز الدهني والإسهال وما ينتج عن ذلك من انخفاض وزن الجسم شائعة.
عادةً ما تظهر المجموعة الكبيرة الثانية من الأعراض في الرئتين: نظرًا لأن المخاط الذي يحدث بشكل طبيعي في الرئتين يكون أكثر لزوجة منه لدى الأشخاص الأصحاء ، فمن الصعب إزالته من الأهداب. هذا يمكن أن يؤدي إلى السعال المزمن وانسداد الشعب الهوائية (توسع القصبات). توفر الكمية الأكبر من إفرازات الرئة أيضًا بيئة جيدة لنمو البكتيريا ، مما يؤدي إلى التهابات الجهاز التنفسي المتكررة والالتهاب الرئوي.
يعالج التليف الكيسي بأعراض طارد البلغم والإنزيمات الهضمية والمضادات الحيوية للعدوى.
يمكنك العثور على المزيد حول هذا على موقعنا تليف كيسي
عامل V Leiden و APC Resistance
تتضمن طفرة العامل الخامس لايدن تغيرًا في المعلومات الجينية التي يمكن أن تسبب زيادة تخثر الدم. والسبب في ذلك هو العامل الخامس في ما يسمى بسلسلة التخثر في الجسم: يضمن مسار الإشارة هذا أنه في حالة الإصابة ، يتم إغلاق الجرح بواسطة "البروتينات اللاصقة" الخاصة بالجسم (الفيبرين). هناك 13 عاملاً في مسار الإشارة هذا ، تمت تسميتها بالأرقام الرومانية (وهذا يعني "العامل الخامس المعاناة"!). للعامل V تأثير مفيد على تكوين سدادة الفيبرين ، ولكن يمكن أيضًا تثبيطه بواسطة ما يسمى بالبروتين المنشط C (APC للاختصار). يلعب هذا دورًا مهمًا في تنظيم مسار الإشارات هذا وفي منع تخثر الدم المفرط.
العامل الخامس الطافر موجود في الأفراد المصابين ولكنه لا يستجيب لـ APC. يفتقر الجسم في هذه المرحلة إلى "جهاز أمان" مهم لمنع تجلط الدم دون سبب ، والذي قد يؤدي حتى إلى انسداد الأوعية الدموية وبالتالي التسبب في اضطرابات الدورة الدموية.
من الناحية الإحصائية ، فإن الأشخاص المتأثرين بطفرة العامل الخامس لايدن هم أكثر عرضة للمعاناة من حدث جلطة (أي جلطة أو انسداد رئوي) ، حتى بدون تاريخ من عوامل الخطر النموذجية. من الناحية الفنية ، يتحدث المرء أيضًا عن "التجلط" ، أي الميل إلى التجلط.
يمكنك العثور على المزيد حول هذا على موقعنا العامل الخامس ليدن
مرض جوشر
في مرض غوشيه ، يتسبب التغيير في معلومات الحمض النووي في حدوث خلل في إنزيم يشارك في استقلاب الدهون ، وبشكل أكثر دقة جلوكوسيريبروسيداز: هذا يساعد في تكسير مكونات الخلايا القديمة. في حالة وجود خلل ، يمكن أن يكون هناك انخفاض في الوظائف أو حتى فقدان الوظيفة ، وبالتالي تظهر الأعراض في مرحلة الطفولة أو الشباب.
تعود أعراض مرض جوشر إلى حد كبير إلى تضخم الكبد والطحال ، حيث يحاول الجسم تعويض نقص الإنزيمات. هذا يزيد من انهيار جميع مكونات الدم ، والتي يمكن التعرف عليها في تعداد الدم واستخدامها كمؤشر تشخيصي مع تضخم الكبد والطحال.
يمكن استخدام إنزيم جلوكوسيريبروسيداز المفقود علاجيًا كدواء. يعتمد تشخيص ومسار مرض جوشر إلى حد كبير على شدة فقدان الإنزيم لوظيفته.
لمزيد من المعلومات ، اقرأ هنا: مرض جوشر.
مرض أوسلر
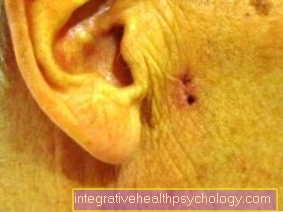
مرض أوسلر هو مرض وراثي يتميز بتوسع الأوعية الدموية الشديد. من حيث المبدأ ، يمكن أن يحدث هذا التوسع في الأوعية في أي مكان ، سواء على الجلد أو على الأعضاء الداخلية. جدران الأوعية المتضخمة رقيقة نسبيًا ويمكن تمزقها بسهولة. نتيجة لذلك ، تنزف المناطق المصابة بسرعة.
يحدث توسع الأوعية بشكل متكرر بشكل خاص على الوجه وفي الغشاء المخاطي للأنف ، لذلك عادة ما يشكو المصابون من نزيف أنفي متكرر ونزيف بقع صغيرة على الوجه.
في حالة الاشتباه في مرض أوسلر ، يجب إجراء التشخيص المناسب ، حيث يمكن أن يحدث توسع الأوعية أيضًا في الأعضاء الحيوية أو الأعضاء ذات إمدادات الدم الجيدة ، مثل الرئتين أو الدماغ أو الكبد ، حيث يكون النزيف من الوعاء الدموي الممزق خطيرًا.
يمكنك العثور على المزيد حول هذا الموضوع على موقعنا مرض أوسلر
مرض ريكلينغهاوزن
الورم العصبي الليفي من النوع الأول - أو مرض ريكلينغهاوزن - هو مرض وراثي يصاب فيه المصابون غالبًا بأورام في خلايا غطاء العصب. يمكن أن تكون الأورام التي تتطور حميدة وخبيثة وتظهر في سن مبكرة.
ومع ذلك ، فإن الأورام النموذجية هي أورام ليفية عصبية حميدة: تتكون من خلايا تغمد العصب وتعزله مثل الكبل الكهربائي ، وكذلك النسيج الضام المحيط. وهي أورام حميدة ، أي أورام غير منتشرة وتنمو ببطء.
ومع ذلك ، قد تكون الجراحة لإزالة الأورام الليفية العصبية أمرًا صعبًا ، لأنها غالبًا ما تكون مرتبطة بقوة بالعصب ومن ثم يجب إزالة العصب المقابل. ومع ذلك ، هذا هو الخيار العلاجي الوحيد للورم الليفي العصبي المصحوب بأعراض ، لأن العلاج السببي لهذا المرض الوراثي غير ممكن.
يمكنك العثور على المزيد حول هذا الموضوع على موقعنا الورم العصبي الليفي من النوع 1
ضمور العضلات
يصف مصطلح الحثل العضلي مجموعة من الأمراض الوراثية التي لا يمكن أو يتعذر فيها تجميع مكونات عضلية معينة بشكل صحيح بواسطة خلايا الجسم. نتيجة لذلك ، عادة ما يصاب الأشخاص المصابون بضعف العضلات في وقت مبكر من الطفولة والمراهقة ، وهذا يمكن أن يؤدي إلى فقدان كتلة العضلات ، والقيود على الحركة وحتى الإعاقات الجسدية.
في حالة الاشتباه في وجود الحثل العضلي ، يجب أولاً تحديد قيم الدم. إذا كانت القيم تتطابق مع التشخيص المشتبه به ، فلا يزال من الممكن إجراء خزعة عضلية: يتم أخذ عينة صغيرة من الأنسجة من العضلات ، ثم يتم فحصها مجهريًا للعيوب الخلوية. من الممكن أيضًا إجراء فحص جيني لتحديد التشخيص ، نظرًا لأن المواقع الجينية المقابلة معروفة عادةً بأشكال مختلفة من الحثل العضلي ويجب تغييرها. لا يُعرف العلاج السببي للحثل العضلي.
يمكنك العثور على المزيد حول هذا الموضوع على موقعنا ضمور العضلات
جفاف الجلد المصطبغ
Xeroderma pigmentosum مرض وراثي نادر لا تعمل فيه بعض الإنزيمات الموجودة في جلد الشخص المصاب. عادةً ما تعتني هذه الإنزيمات بإصلاح الحمض النووي ، والذي يمكن أن يتلف بسبب ضوء الشمس أو ضوء الأشعة فوق البنفسجية. يمكن أن يتسبب تلف الأشعة فوق البنفسجية في الإصابة بسرطان الجلد لدى الأشخاص المصابين وكذلك في جميع الأشخاص الآخرين ، ولكن مع جفاف الجلد المصطبغ ، تتسارع العملية بسبب نقص آليات الإصلاح. نتيجة لذلك ، يصاب الأشخاص المصابون بأشكال حادة من سرطان الجلد في مرحلة الطفولة والمراهقة وبعد تعرض قصير لأشعة الشمس.
العلاج السببي غير ممكن بعد. يجب أن يتجنب الأشخاص المصابون ضوء الشمس مدى الحياة ، وهذا هو السبب في أن لقب "أطفال ضوء القمر" قد رسخ نفسه للأشخاص المتضررين (في بعض الأحيان الصغار جدًا). بالإضافة إلى ذلك ، يجب أن يشرف طبيب الأمراض الجلدية على هؤلاء الأشخاص لإجراء فحوصات منتظمة لسرطان الجلد من أجل إزالة سرطان الجلد المتطور حديثًا على الفور إذا تم اتباع هذه الإجراءات بدقة ، فإن متوسط العمر المتوقع للشخص المصاب بجفاف الجلد المصطبغ هو نفس متوسط العمر المتوقع للشخص غير المصاب.
يمكنك العثور على المزيد حول هذا المرض على موقعنا جفاف الجلد المصطبغ
متلازمة لينش
متلازمة لينش هي تغير في الحمض النووي يسبب خلل في إنزيم في خلايا الجسم.في الأشخاص المصابين ، تكون هناك آلية معينة معيبة ، والتي من المفترض أن تحمي الخلايا من التنكس ، أي النمو غير المنضبط - وبالتالي فإن الأشخاص المصابين بمتلازمة لينش لديهم خطر متزايد للإصابة بالسرطان.
غالبًا ما يحدث سرطان القولون لأن الخلايا غالبًا ما تنقسم هنا على أي حال ، وتصبح الأخطاء في برمجة النمو والموت للخلية واضحة بشكل أسرع. غالبًا ما يصاب الأشخاص المصابون بورم في الأمعاء الغليظة في سن مبكرة بشكل غير معتاد ، أي قبل سن الخمسين ، والذي يُطلق عليه فيما بعد HNPCC (سرطان القولون الوراثي غير السليلي). ومع ذلك ، ليس كل من لديه التركيب الجيني لمتلازمة لينش سيصاب بسرطان القولون. من ناحية أخرى ، يمكن للأعضاء الأخرى أيضًا أن تتطور إلى ورم ، حيث أن الاستعدادات الجينية التي تفضل تطور الورم موجودة في جميع خلايا الجسم. لذلك ، من الضروري إجراء فحوصات منتظمة وفحوصات وقائية للأشخاص المصابين بمتلازمة لينش من أجل علاج الأورام التي تظهر في مرحلة مبكرة بشكل مناسب.
يمكنك العثور على المزيد حول هذا الموضوع على موقعنا متلازمة لينش




.jpg)