التربسينوجين
التعريف - ما هو التربسينوجين؟
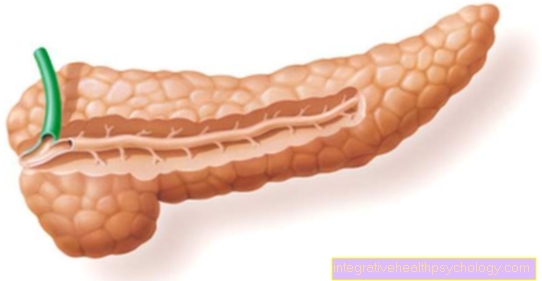
التربسينوجين هو السلائف غير النشطة ، ما يسمى طليعةوهو إنزيم يصنع في البنكرياس ويسمى البنكرياس. جنبا إلى جنب مع إفراز البنكرياس المتبقي ، ما يسمى البنكرياس ، يتم إطلاق التربسينوجين الإنزيم عبر قنوات البنكرياس في الاثني عشر ، جزء من الأمعاء الدقيقة. هذا هو المكان الذي يتم فيه تنشيط إنزيم التربسين.
يسمى هذا الانزيم "هيدرولاز"مصنفة ، أي أنها قادرة على فصل الروابط بين الأحماض الأمينية الفردية. تحدث هذه العملية في الأمعاء الدقيقة بدلاً من ذلك ، يقوم بتقسيم البروتينات التي يتم تناولها من خلال الطعام إلى أجزاء أصغر من الأحماض الأمينية ، مما يمكّن الجسم من امتصاصها.

كيف يتم تفعيل التربسين؟
يمكن أن يتم تنشيط التربسينوجين للتربسين بطريقتين مختلفتين. في كلا الاتجاهين ، لا يتم التنشيط في منطقة البنكرياس أو مجاريه ، ولكن فقط في منطقة الاثني عشر ، وهي جزء من الأمعاء الدقيقة.
- مطلوب إنزيم آخر لإمكانية تنشيط التربسين. يتم إنتاج هذا الإنزيم في حدود الفرشاة ، أي الخلايا السطحية للاثني عشر. تسمى إنتيروبيبتيداز أو إنتيروكيناز. الانزيم من بين هيدرولاز مصنفة. هذا يعني أنه يمكنهم شطر مركبات الأحماض الأمينية الفردية بشكل عكسي ، والتي تعطي مركب التربسينوجين الإنزيم ، عن طريق استهلاك جزيئات الماء. عندما يتم تنشيط التربسينوجين إلى التربسين ، تنفصل سلسلة من ستة أحماض أمينية ، تسمى هيكسابيبتيد ، عن إنزيم التربسينوجين أثناء تناول الماء. هذا يخلق سلسلة من الأحماض الأمينية مختصرة مقارنة بالسابق. هذه العملية تسمى تحلل البروتين المحدود. ومع ذلك ، فإن الإنزيم الآن في شكله النشط ويمكنه تقسيم المزيد من سلاسل الأحماض الأمينية من أجل التمكن من تكسير وهضم البروتينات.
- البديل الثاني لتنشيط التربسينوجين للتربسين يمثله إنزيم التربسين النشط بالفعل. لا يستطيع التربسين فقط تقسيم البروتينات الأجنبية إلى سلاسل أحماض أمينية أصغر ، ولكن يمكنه أيضًا تقصير بروتوكولات الجسم مثل التربسينوجين بواسطة العديد من الأحماض الأمينية. يحب التربسين بشكل خاص الانقسام بعد الحمض الأميني السادس من التربسينوجين. هذا يعني أن سداسي الببتيد ينفصل ، مما يحول التربسينوجين إلى شكله النشط ، التربسين. بالإضافة إلى التربسينوجين ، يمكن أن يحول التربسين النشط ثلاثة إنزيمات أخرى مهمة للهضم إلى شكلها النشط. هناك عاملان غير واضحين في البداية مهمان أيضًا للتنشيط. من ناحية أخرى ، يكون تأثير التربسين جيدًا بشكل خاص عند قيمة الأس الهيدروجيني الأساسية قليلاً من 7 إلى 8 ، مما يعني أن التربسينوجين ينشط بشكل متزايد. من ناحية أخرى ، يتم إطلاق التربسينوجين في البنكرياس باستخدام مثبط التربسين. هذا يمنع التنشيط المبكر داخل البنكرياس ويتفكك فقط في الاثني عشر.
أين يتم صنع التربسينوجين؟
تتم صياغة إنزيم التربسينوجين بشكل تقريبي في البنكرياس. هذه أكاذيب عبر الجزء العلوي من البطن إلى يسار المعدة. لا يزال من الممكن تقسيم البنكرياس إلى قسمين:
- من جزء الغدد الصماء تنتج هرمونات مثل الأنسولين لتنظيم توازن السكر الذي يعمل داخل الجسم.
- من جزء خارجيالذي يشكل الجزء الأكبر من البنكرياس ، ينتج البنكرياس ، وهو الإنزيم التربسينوجين ويلعب دورًا مهمًا في الهضم.
قد تكون مهتم ايضا ب: وظائف البنكرياس
ما هي القيم الطبيعية؟
نظرًا لأن التربسينوجين ينتقل عادة مباشرة إلى الأمعاء الدقيقة عبر قنوات البنكرياس ، فعادة لا يوجد التربسينوجين في الدم ، مما يعني أن القيم الطبيعية تقترب من الصفر.
إذا تم اكتشاف التربسينوجين في الدم ، فإن النتيجة تتحدث بالتأكيد عن عملية مرضية. هنا ، على سبيل المثال ، تأتي مشكلة حادة التهاب البنكرياس و أ تليف كيسي في السؤال. يتم اختبار التربسين كجزء من فحص حديثي الولادة.
ما علاقة التربسينوجين بالتليف الكيسي؟
في التليف الكيسي ، يُسمى أيضًا التليف الكيسي ، ينتج عن حدوث طفرة في الجينوم تغيير في تكوين إفراز الغدد التي تطلق إفرازها إلى سطح الجسم مثل الأمعاء. يصبح الإفراز أكثر لزوجة بشكل ملحوظ ، مما يعني أنه يمكن إطلاقه بشكل أبطأ.
هذا مهم بشكل خاص في حالة البنكرياس. نظرًا لطول فترة الإقامة في ممرات البنكرياس ، يكون للإفراز تأثير متزايد داخل العضو. نظرًا لأنه يتم أيضًا تنشيط التربسينوجين بشكل متزايد للتربسين ، يحدث هضم الجسم ، مما قد يؤدي إلى التهاب البنكرياس الحاد.
يمكن العثور على مزيد من المعلومات حول هذا الموضوع هنا: تليف كيسي
ما هو التربسين؟
التربسين هو إنزيم ينشأ من طليعة غير نشطة ، إنزيم التربسينوجين ، ويلعب دورًا مهمًا في هضم البروتينات. يأتي إنزيم التربسينوجين من الجزء الخارجي من البنكرياس. يتم تنشيط هذا الإنزيم بطريقتين مختلفتين. من ناحية ، بمساعدة إنزيم إنتيروبيبتيداز ، يتم فصل سلسلة الأحماض الأمينية المكونة من ستة أحماض أمينية. من ناحية أخرى ، يمكن أن ينشط التربسين نفسه. هنا أيضًا ، يتم فصل سلسلة الأحماض الأمينية المكونة من ستة أحماض أمينية. يمكن أن يقوم التربسين النشط أيضًا بعمل الإنزيمات الثلاثة بروكاربوكسي ببتيداز, Proaminopeptidases و كيموتربسينوجين تحويل إلى ثلاثة إنزيمات نشطة عن طريق فصل سلسلة الأحماض الأمينية. تشارك هذه الإنزيمات الثلاثة أيضًا في هضم البروتينات.
يصنف التربسين على أنه إنزيم تحت فئة هيدرولاز مصنفة. هذا يعني أنه يمكنهم تقسيم الروابط بين الأحماض الأمينية بشكل عكسي عن طريق استهلاك الماء. تصل القدرة على تقسيم سلاسل الأحماض الأمينية إلى الحد الأقصى في البنكرياس الأساسي قليلاً مع قيم الأس الهيدروجيني بين 7 و 8. هذه الخاصية ضرورية لعملية الهضم.
بعد الإنزيمات الموجودة في لعاب الفم ، يمثل التربسين الخطوة الثانية في تكسير البروتينات.لا يقطع الإنزيم سلسلة الأحماض الأمينية للبروتينات من الخارج ، بل يقسم السلسلة بأكملها إلى عدة أجزاء صغيرة ، والتي يتم تقصيرها بعد ذلك بواسطة إنزيمات أخرى بحيث تكون يمكن امتصاصه في الجسم من خلال الغشاء المخاطي المعوي.
ويمكن الاطلاع على مزيد من المعلومات هنا: التربسين
ماذا يحدث لنقص التربسين؟
مع نقص التربسين ، يتعطل هضم البروتينات. في ما يلي ، يتم امتصاص عدد أقل من الأحماض الأمينية في الجسم. نظرًا لأن بعض الأحماض الأمينية ضرورية لجسم الإنسان ، حيث لا يمكن إنتاجها عن طريق تعديل الأحماض الأمينية الموجودة ولا عن طريق تركيبها ، فإن أعراض النقص تحدث بعد مرور بعض الوقت ، والتي إذا تُركت دون علاج يمكن أن يكون لها عواقب وخيمة.
وقد يحدث أيضًا أن يتم استخدام مخازن الأحماض الأمينية في الجسم ، مثل البروتينات الموجودة في العضلات ، مما يؤدي إلى فقدان الوزن وتقليل المرونة.
نقص ألفا 1 أنتيتريبسين
غالبًا ما يحدث نقص ألفا -1 أنتي تريبسين بسبب عيب وراثي. Alpha-1-antitrypsin هو إنزيم يمنع الإنزيمات الأخرى من العمل. عادة ما يكون للإنزيمات المثبطة في هذه العملية مهمة تكسير البروتينات ، مما يجعلها تفقد وظيفتها. وبالتالي ، يمكن أيضًا استخدام Alpha-1-Antitrypsin مثبط البروتين تم تعيينه.
تحدث الإنزيمات المثبطة بواسطة Alpha-1-Antitrypsin بشكل رئيسي في العمليات الالتهابية وهي بشكل أساسي كيموتربسين ، التربسين ، البلازمين ، الإيلاستاز و الثرومبين.
إن تثبيط الإيلاستاز له أهمية خاصة هنا. كقاعدة عامة ، يكسر الإيلاستاز الإيلاستين ، الموجود بشكل رئيسي في الرئتين. الإيلاستين هو بروتين هيكلي مسؤول إلى حد كبير عن مرونة الرئتين. إذا كان هناك نقص في مثبطات الإيلاستاز مثل alpha-1-antitrypsin ، فقد يؤدي ذلك إلى زيادة نشاط الإيلاستاز في الرئتين. هنا ، مثل أي مكان آخر في الجسم ، يكسر الإيلاستاز البروتينات ، لكن هذا يؤثر على أنسجة الجسم في الرئتين. هذا يؤدي إلى تلف كبير في أنسجة الرئة ، مما يحد حتما من وظائف الرئة. تشمل الأعراض التي تتطور منه سعال وضيق في التنفس وضيق في الشعب الهوائية. بالإضافة إلى ذلك ، يمكن للكبد ، المسؤول بشكل أساسي عن إنتاج الإيلاستاز ، أن يُظهر قيمًا مرتفعة للكبد ويتعرض لمزيد من التلف بسبب الاحتقان الصفراوي.
ويمكن الاطلاع على مزيد من المعلومات هنا: نقص ألفا 1 أنتيتريبسين
توصيات من فريق التحرير لدينا
- التربسين
- ألفا 1 أنتيتريبسين
- نقص ألفا 1 أنتيتريبسين
- الكيموتريبسين - ما هو مهم؟
- دور الانزيمات في جسم الانسان